高效裂解多重耐药金黄色葡萄球菌噬菌体YNP1生物学特性研究(三)
2.2.6 噬菌体的最佳感染复数
将宿主菌与噬菌体混合培养2h后测定噬菌体滴度(表2)。结果显示,当MOI=1时,噬菌体滴度最高,所以噬菌体的最佳感染复数为1。
| 编号 | 细菌数 (CFU/mL) | 噬菌体数 (PFU/mL) | 感染复数 (MOI) | 噬菌体滴度 (PFU/mL) |
|---|---|---|---|---|
| 1 | 1×108 | 1×108 | 0.01 | 1.61×108 |
| 2 | 1×108 | 1×107 | 0.1 | 1.68×108 |
| 3 | 1×109 | 1×108 | 1 | 5.70×108 |
| 4 | 1×109 | 1×109 | 10 | 2.81×109 |
| 5 | 1×107 | 1×108 | 100 | 2.80×108 |
2.2.7 噬菌体的一步生长曲线
通过oCelloScope系统测定的一步生长曲线如图3E所示。系统自动分析显示,噬菌体YNP1的潜伏期约为10 min,裂解期持续约50 min,暴发量经软件计算为71 PFU/感染细胞。该曲线由系统连续监测生成,数据点更密集,能更精确地反映裂解动力学过程。
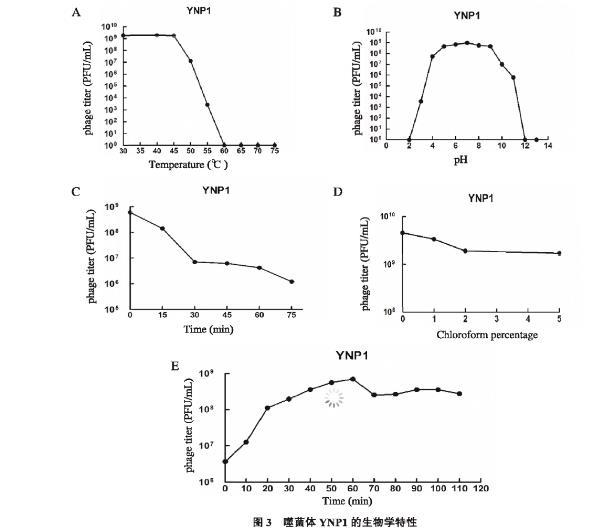
图3 噬菌体YNP1的生物学特性
A:噬菌体YNP1的热稳定性;B:噬菌体YNP1的最适pH测定;C:噬菌体YNP1对紫外线的敏感性;D:噬菌体YNP1对氯仿敏感性测定;E:噬菌体YNP1的一步生长曲线
2.2.8 噬菌体全基因组序列分析和裂解酶基因的挖掘
使用PHAST软件和NCBI BLAST软件对噬菌体全基因组序列进行分析,结果显示噬菌体YNP1基因组长度为143.5 kb,(G+C)%含量为30.80%,A、T、G、C含量分别为31.46%、37.74%、13.67%、17.14%,有205个开放阅读框(open reading frames, ORFs)。其中142个为假定蛋白(hypothetical protein)序列,对63个ORFs的同源性比较及功能预测分析,筛选到一个裂解酶基因,预测该基因表达的蛋白同时具有酰胺酶催化结构域和SH3b结合结构域(图4),命名为LysYNP1。通过对国内外已经发表的噬菌体编码裂解酶的结构和组成分析发现,具有酰胺酶催化域的裂解酶一般活性较高,而具有SH3b结合域的裂解酶一般会呈现相对较宽的裂解谱。同时在该噬菌体的全基因组序列中未发现潜在的毒力基因与整合酶基因,表明该噬菌体满足其作为治疗性噬菌体的前提要求。
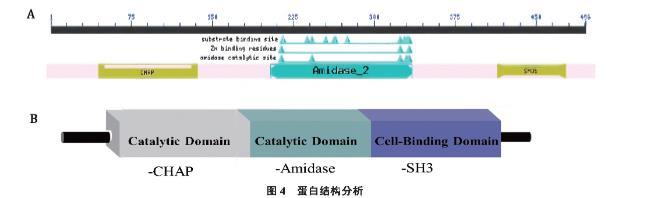
图4 蛋白结构分析
A:软件预测裂解酶结构;B:葡萄球菌噬菌体裂解酶的结构
2.3 裂解酶的表达
2.3.1 裂解酶LysYNP1的诱导表达
取表达菌株培养至OD600达到0.6时加入诱导剂IPTG至终浓度为1 mmol/L,25℃诱导12 h,进行SDS-PAGE电泳检测融合蛋白表达情况。结果显示,诱导后上清液在55 kDa处有一条明显的蛋白条带,诱导后沉淀、未加诱导剂组和空载体组均未出现条带(图5)。
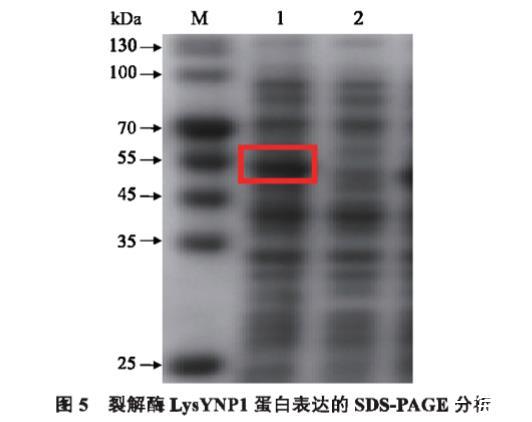
图5 裂解酶LysYNP1蛋白表达的SDS-PAGE分析
M:蛋白质相对分子质量标准;1:pET28a-LysYNP1诱导后上清液;2:pET28a-LysYNP1诱导前
2.3.2 裂解酶LysYNP1的活性检测与裂菌谱测定
以15株金黄色葡萄球菌为指示菌,采用平板裂解实验检测LysYNP1的活性以及裂菌谱。A、B孔分别加入90 μL LysYNP1和LysJD,C孔加入等量的PBS为阴性对照。结果显示A、B孔能够形成透亮的裂菌圈,C孔不能形成裂菌圈(图6)。裂解酶能够裂解多株MRSA菌株以及患乳腺炎的乳汁中分离的多重耐药金黄色葡萄球菌,裂菌谱如表3所示,结果显示,LysYNP1的裂菌谱比LysJD更广。
通过oCelloScope系统对裂解酶LysYNP1粗提液进行的实时活性监测显示,在加入裂解酶后,宿主菌液的生物量在60-90分钟内迅速下降,并形成典型的裂解曲线。系统生成的剂量依赖曲线表明,裂解酶的活性在一定浓度范围内与裂解速率呈正相关。

图6 检测LysYNP1粗提液的裂解活性
A:加入90 μL LysYNP1粗提液;B:加入90 μL LysJD粗提液;C:加入90 μL PBS
3 讨论
随着人们对新型抗菌药物的迫切需求,噬菌体治疗重新回到人们的视野。噬菌体是一类细菌特异性病毒,具有安全、高效等优势,这使其在防控耐药菌株感染方面具有巨大的应用潜力。本研究从污水样本中分离到一株噬菌体,命名为vB_SauM_YNP1,该噬菌体可以裂解多株从乳汁中分离的MRSA菌株,形成透亮的噬斑。在裂菌谱实验中,我们发现该噬菌体不仅可以裂解金黄色葡萄球菌,还可以裂解其他葡萄球菌,包括一株鸡葡萄球菌,而这株鸡葡萄球菌也是从患病奶牛的乳汁中分离到的,本研究对该鸡葡萄球菌进行了药敏试验,发现其也是一株多重耐药菌。因此本研究分离得到的噬菌体具备防控耐药葡萄球菌的潜在价值。
在双层平板实验和斑点实验中,我们发现裂解结果并不完全一致,斑点实验能够出现晕环,但双层平板实验并没有透亮的噬斑,提示我们该噬菌体可能具有合成细胞壁水解酶的特性。裂解革兰氏阳性菌的噬菌体内通常具有两种类型的细胞壁水解酶,一种称为解聚酶,解聚酶是一种能够降解细菌多糖成分的酶,主要作用是特异性裂解宿主菌细胞壁上的多糖成分,帮助噬菌体抵达细菌细胞膜表面,进而提高杀菌作用;另一类称为裂解酶,裂解酶是噬菌体侵染细菌后期合成的细胞壁肽聚糖水解酶,它作用于细菌的细胞壁肽聚糖,致使细胞壁肽聚糖连接键断裂,最终导致细菌裂解。我们对噬菌体YNP1的全基因组进行了分析,筛选出一个裂解酶基因,我们将该裂解酶进行了表达,通过平板裂解实验,发现8~12h内该裂解酶可以形成半透明的晕圈,并且随着作用时间的增加裂菌圈逐渐扩大且透明清晰,这与Cornelissen等的研究结果是一致的。同时我们发现该裂解酶的裂菌谱比其噬菌体自身以及实验室制备保存的能够高效裂菌的裂解酶LysJD的裂菌谱更广,并且与噬菌体相比,裂解酶具有特异性强、高效快速、安全性高、不易诱导细菌产生耐药性等优势,因此该裂解酶很有可能成为治疗奶牛乳腺炎的一种新型抗菌药物。
相关新闻推荐
1、新的微生物种间和跨界相互作用模式——操控自身的抗真菌化合物抑制邻近真菌的生长
2、溶藻弧菌噬菌体φV039C一步生长曲线等生物学特性的研究——实验结果与分析
3、长期使用氯己定CHX预防龋齿,会导致变形链球菌产生耐药性吗
