碳青霉烯类耐药革兰阴性菌联合药敏试验方法学、流程、优缺点和结果判读(三)
7.4纸片扩散法
7.4.1常规纸片扩散法将含有定量抗菌药物的纸片贴在已接种测试菌的琼脂表面上,纸片中的药物吸收琼脂中的水分后向纸片周围扩散,随着扩散距离的增加抗菌药物的浓度呈对数减少,在纸片的周围形成递减浓度梯度。在纸片周围抑菌浓度范围内的测试菌不能生长,而抑菌浓度范围外的菌株则继续生长,从而在纸片的周围形成抑菌圈。操作时将两张不同抗菌药物的药敏纸片以一定的距离放置,参考距离为一张纸片的边缘距离另外一张纸片的抑菌圈边缘3~4 mm。经过孵育后根据两药间的抑菌圈扩大或缩小等现象,判断两药是否存在协同、相加、无关或拮抗现象(图7和图8)。纸片扩散法具有操作简单且价格低廉的特点,但缺点是结果不易阅读。纸片扩散法联合药敏试验两药敏纸片的距离可参考图8。若常规纸片扩散法联合药敏试验结果模糊,难以判断,建议使用其他方法(如肉汤微量稀释棋盘法、纸条法)进行确认。
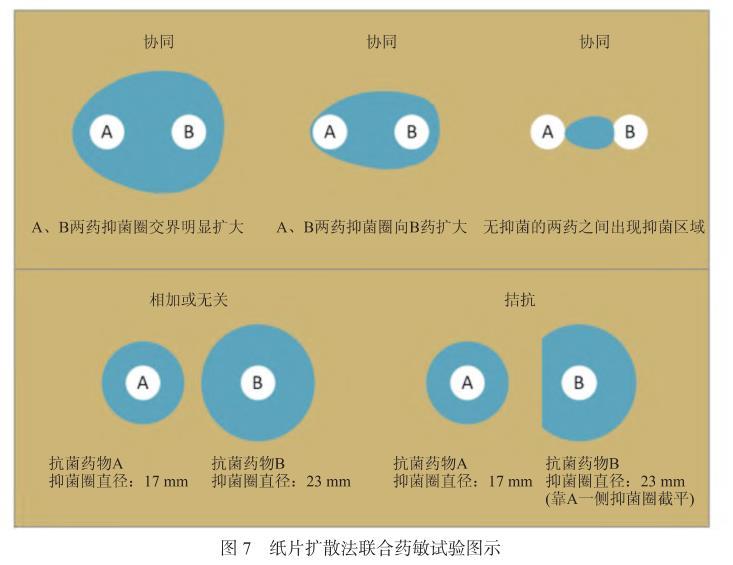
图7纸片扩散法联合药敏试验图示
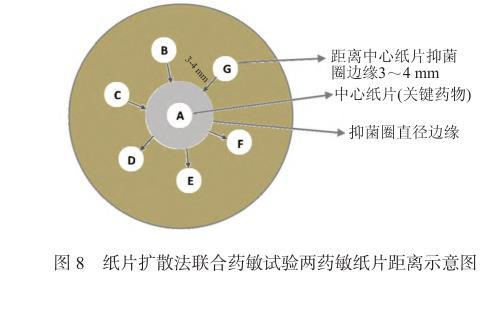
图8纸片扩散法联合药敏试验两药敏纸片距离示意图
优先选择敏感的抗菌药物A作为关键药物与其他抗菌药物进行联合,如头孢他啶-阿维巴坦、替加环素或多黏菌素。
7.4.2纸片优加法纸片优加法[32]为常规纸片扩散法的改良方法。实验时按图示先将2张含抗菌药物A单药和1张含抗菌药物B单药纸片贴在已接种菌液的MH琼脂表面,3张纸片间的中心距离为25 mm。放置30 min后,待纸片中的抗菌药物完全渗透入琼脂中后,按图示移去一张A纸片,再在相同的位置上覆盖贴上抗菌药物B单药纸片。经孵育后阅读抑菌圈直径,见图9。
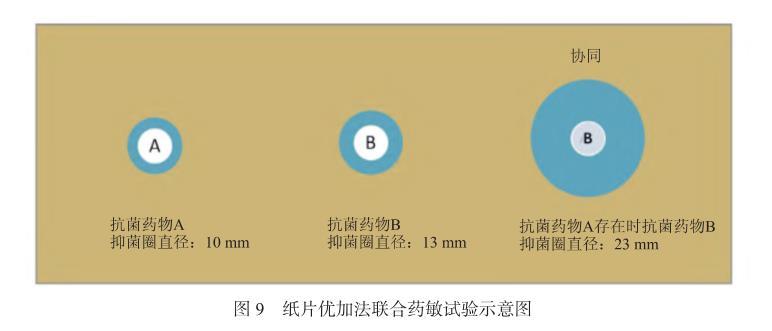
图9纸片优加法联合药敏试验示意图
专家共识八:两药协同定义为抗菌药物A和抗菌药物B单药均为耐药,但抗菌药物B在抗菌药物A存在时表现为敏感或中介(即两药联合的抑菌圈直径明显大于任何单药抑菌圈直径)。
7.4.3改良纸片优加法本方法与纸片优加法原理相似,目的为增加有效抗菌药物的含量,达到加大剂量实现抑菌或杀菌的目的,如常可用此法增加头孢哌酮-舒巴坦对CRAB的抗菌活性。操作方法同常规纸片扩散法,唯一的不同之处为多张同一抗菌药物纸片紧邻贴在一起,以实现该区域该抗菌药物浓度加量的目的。由于舒巴坦对鲍曼不动杆菌存在杀菌活性,增加舒巴坦剂量可明显提高鲍曼不动杆菌对头孢哌酮-舒巴坦的敏感率[22],可尝试以头孢哌酮-舒巴坦为基础联合舒巴坦的联合药敏试验方案。见图10。
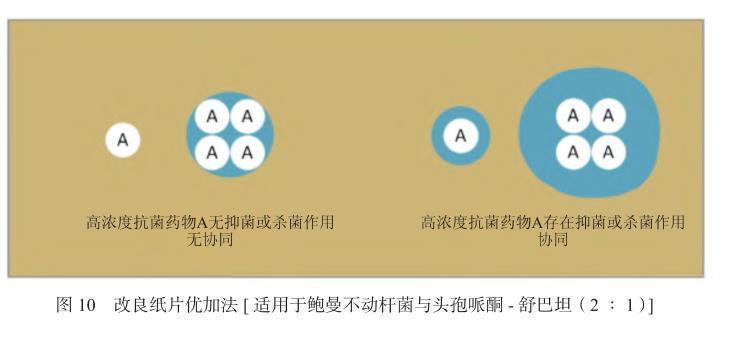
图10改良纸片优加法[适用于鲍曼不动杆菌与头孢哌酮-舒巴坦(2∶1)]
7.4.4肉汤纸片洗脱法肉汤纸片洗脱法[32]为改良肉汤稀释法,包括两种方法。
①常规肉汤纸片洗脱法:此方法为两种不同抗菌药物的联合。实验时在4根无菌试管中分别加入2 mL的CAMHB肉汤,分别标记为C、A、B和A+B管,其中C管为生长对照,A管放入1张抗菌药物A药敏纸片,B管放入1张抗菌药物B药敏纸片,A+B管同时放入抗菌药物A和抗菌药物B药敏纸片,轻轻涡旋30 s,室温(23±2)℃孵育至少30 min使纸片中的抗菌药物完全扩散入肉汤中(不可超过60 min)(参考CLSI黏菌素肉汤纸片洗脱试验)[35]。然后准备0.5麦氏浊度待测菌菌悬液,用移液器分别在在C、A、B和A+B管中加入10μL的0.5麦氏浊度待测菌菌悬液,最终接种菌量为7.5×105CFU/mL,35℃孵育16~20 h后观察各管中的细菌生长情况(图11)。注意:本方法每试管中肉汤的体积需按每片药敏纸片中所含抗菌药物的量和该菌对该抗菌药物的耐药判断标准而定,溶液中抗菌药物最终浓度应≥中介标准。如该菌对抗菌药物的耐药标准为≥16 mg/L,药敏纸片中所含抗菌药物的量为30μg/片,则每管中CAMHB肉汤的含量应为2 mL。以纸片中抗菌药物完全溶解入肉汤中计算,2 mL肉汤中该抗菌药物的浓度为15 mg/L(近似于耐药标准)。
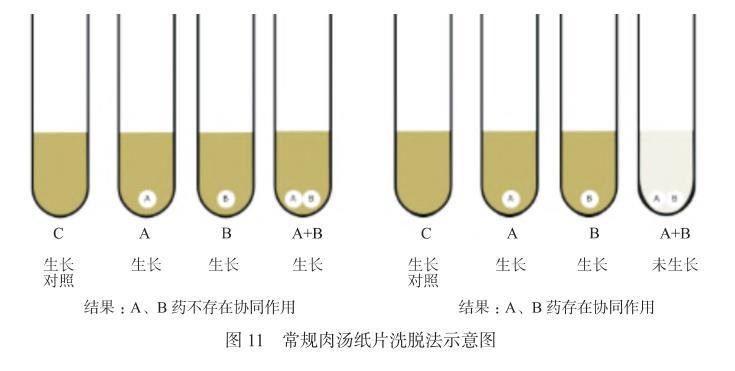
图11常规肉汤纸片洗脱法示意图
专家共识九:若C、A和B管中细菌均生长,但A+B管无细菌生长,报告抗菌药物A和抗菌药物B联合“存在协同作用”。
专家共识十:若C、A、B和A+B管中的细菌均生长,报告抗菌药物A和抗菌药物B“不存在协同作用”。
举例:如该菌为产金属酶肺炎克雷伯菌,抗菌药物A所含药物为头孢他啶-阿维巴坦,抗菌药物B所含药物为氨曲南。结果显示单药时细菌均生长,但两药联合后细菌生长被抑制,呈现协同抑菌或杀菌作用。
②改良肉汤纸片洗脱法:此方法为单种抗菌药物增加剂量的试验。实验时在4根无菌试管中分别加入2 mL的CAMHB肉汤,分别标记为C、A、A×2和A×3,其中C管为生长对照,A管放入1张抗菌药物A药敏纸片,A×2管放入2张抗菌药物A药敏纸片,A×3管放入3张抗菌药物A药敏纸片,轻轻涡旋,室温孵育至少30 min使纸片中的抗菌药物完全扩散入肉汤中(不可超过60 min)(参考CLSI黏菌素肉汤纸片洗脱试验)[35]。然后吸取10μL的0.5麦氏浊度待测菌菌悬液分别加入C、A、A×2和A×3管中,最终接种菌量为7.5×105CFU/mL,35℃孵育16~20 h后观察各管中的细菌生长情况(图12)。注意:本方法每试管中肉汤的体积需按每片药敏纸片中所含抗菌药物的量和该菌对该抗菌药物的耐药判断标准而定,溶液中抗菌药物最终浓度应≥中介标准。如该菌对抗菌药物的耐药标准为≥16 mg/L,药敏纸片中所含抗菌药物的量为30μg/片,则每管中CAMHB肉汤的含量应为2 mL。以纸片中抗菌药物完全溶解入肉汤中计算,2 mL肉汤中该抗菌药物的浓度为15 mg/L(近似于耐药标准)。
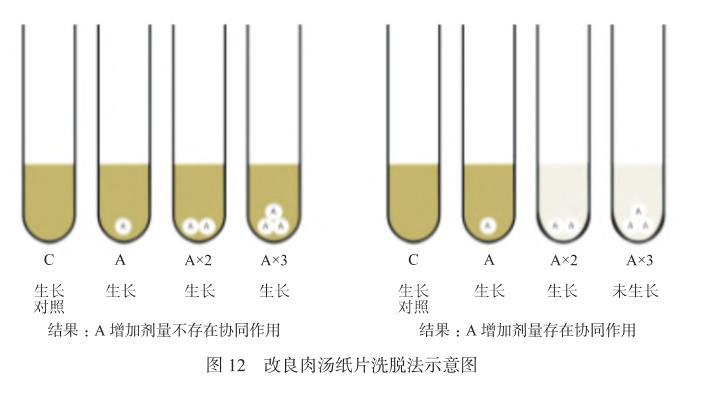
图12改良肉汤纸片洗脱法示意图
专家共识十一:若C和A管细菌均生长,但A×2和A×3管细菌均未生长,报告抗菌药物A增加剂量“存在协同作用”。
专家共识十二:若C、A、A×2和A×3管细菌均生长,报告抗菌药物A增加剂量“无协同作用”。
7.5联合杀菌曲线[16-17,24,36-37]
通过检测暴露于单药或联合药物不同时间段时的细菌存活数,评估不同药物间的协同或拮抗作用(图13)。协同通常定义为:与最具抗菌活性的单药相比,联合用药后细菌数呈≥2 log10CFU/mL级别的下降;拮抗通常定义为:与最具抗菌活性的单药相比,联合用药后细菌数呈≥2 log10CFU/mL级别的上升。
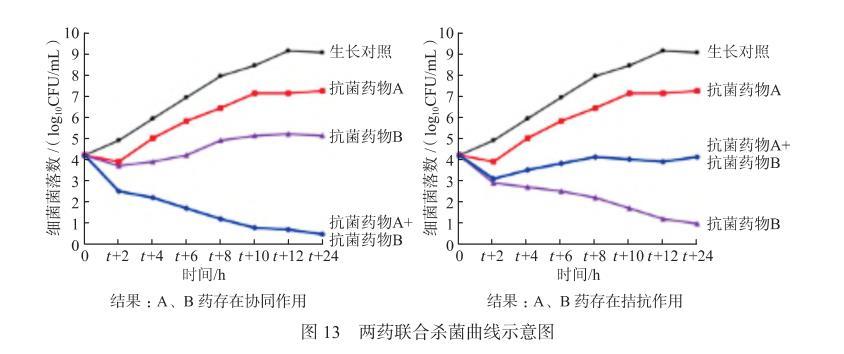
图13两药联合杀菌曲线示意图
8联合药敏试验结果报告及相关注释
不同联合药敏试验方法所得结果,报告格式略有差异。
以出现协同作用为例,当采用金标准方法进行联合药敏试验时,若抗菌药物A和抗菌药物B两药呈现协同作用,可报告:抗菌药物A和抗菌药物B联合存在协同作用。当采用非金标准方法进行联合药敏试验时,若抗菌药物A和抗菌药物B两药呈现协同作用,可报告:抗菌药物A和抗菌药物B联合可能存在协同作用。
专家共识十三:采用肉汤微量稀释棋盘法及纸条交叉法联合药敏试验,可根据FIC指数判断两药协同、相加、无关和拮抗结果。若采用其他方法开展联合药敏试验,仅根据结果报告两药是否存在协同作用。见图14、图15。
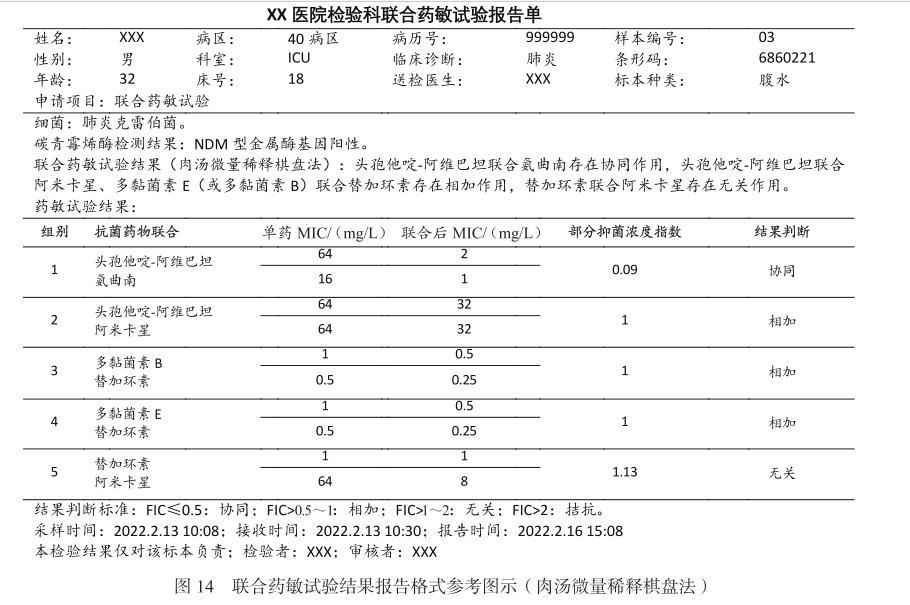
图14联合药敏试验结果报告格式参考图示(肉汤微量稀释棋盘法)
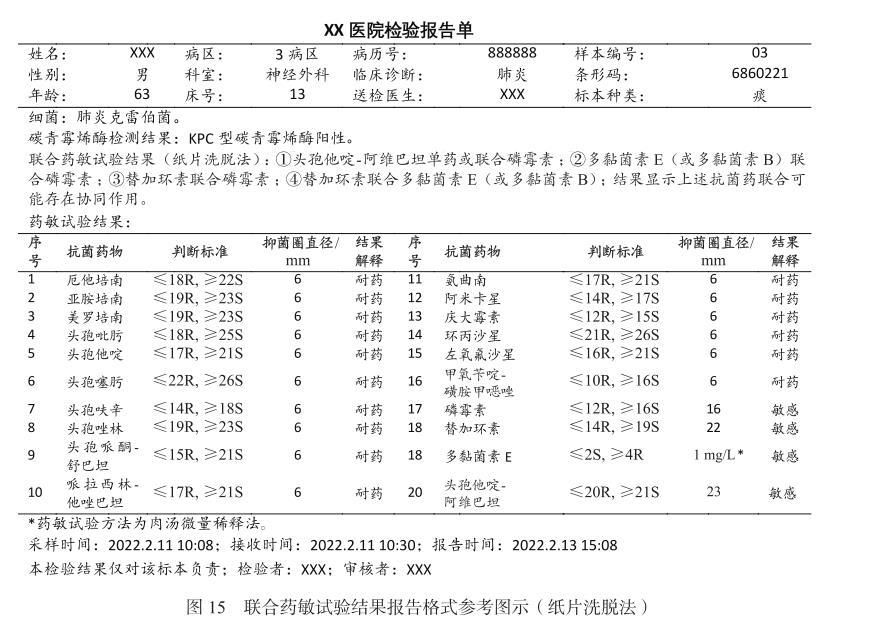
图15联合药敏试验结果报告格式参考图示(纸片洗脱法)
9质量控制
目前国际上无专用的联合药敏试验质量控制要求,建议可按照CLSI文件推荐的稀释法(MIC测定)或纸片扩散法的质控要求[35],规范联合药敏试验所涉及的稀释法和纸片扩散法等重要方法学的操作步骤、材料、试剂和质控菌株的要求进行质控,各实验室宜根据自己实验室的条件,针对所选择的联合药敏方法进行质量控制或性能验证,仅在所有涉及的联合药敏试验环节均在控的前提下,方可开展联合药敏试验。
相关新闻推荐
1、Biosense微生物动态监测系统实验操作步骤——脓肿分枝杆菌的生长曲线
2、实时监测蓝藻细胞内用于外源生物合成的苯丙氨酸相对含量的方法
