不同霉变时期肉豆蔻饮片需氧菌、霉菌、酵母菌菌落总数统计(二)
2.3.2霉菌、酵母菌培养基适用性试验
分别移取黑曲霉、白色念珠菌菌液1 mL(含菌量50-100 cfu)至灭菌平皿中,分别倾倒沙氏葡萄糖琼脂培养基、沙氏葡萄糖琼脂对照培养基15 mL,待其凝固后,倒置于恒温培养箱中20-25℃培养72 h。每个菌种每种类型培养基各做3个平行。测定菌落数。
被检固体培养基上的菌落平均数与对照培养基上的菌落平均数比值应在0.5-2范围内,且菌落形态大小与应与对照培养基上的菌落一致。结果(表2,图3),被检固体培养基上的菌落平均数与对照培养基上的菌落平均数均在0.5-2范围内。被检固体培养基上菌落形态大小与对照培养基上的菌落一致。
2.4计数方法适用性试验
2.4.1需氧菌总数计数方法适用性试验
试验组:分别移取1∶1000、1∶10000、1∶100000供试液9.9 mL于灭菌试管中,加入制备好的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉及白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu。从试管中移取1 mL至灭菌平皿中,立刻倾注胰酪大豆胨琼脂培养基,待其凝固后倒置于霉菌培养箱中30-35℃培养48 h。每个菌种平行制备2个平皿,测定试验组菌落数。

图3 a黑曲霉;b白色念珠菌
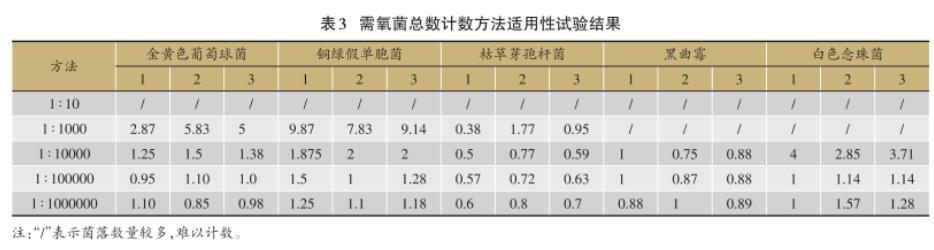
表3需氧菌总数计数方法适用性试验结果
供试品对照组:分别移取1∶1000、1∶10000、1∶100000供试液9.9 mL于灭菌试管中,加入0.1 mL无菌生理盐水,其余按试验组操作。测定供试品对照组菌落数。
菌液对照组:取9.9 mL无菌生理盐水于灭菌试管中,加入与试验组相同的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉及白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu,其余按试验组操作。测定菌液对照组菌落数,进行微生物回收试验。
阴性对照组:移取1 mL无菌生理盐水于灭菌平皿中,其余按试验组操作。平行制备2个平皿。
按回收率=[(试验组平均菌落数-供试品对照组平均菌落数)/菌液对照组平均菌落数]计算回收率,结果(表3)。根据2015年版《中国药典》,采用平皿法时,回收率应在0.5-2范围内。可得出,金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉需稀释至1∶10000,白色念珠菌需稀释至1∶100000方能达到回收率要求。
2.4.2霉菌、酵母菌总数计数方法适用性试验
分别移取1∶10000、1∶100000、1∶1000000供试液9.9 mL于灭菌试管中,加入制备好的黑曲霉、白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu。从试管中移取1 mL至灭菌平皿中,立刻倾注沙氏葡萄糖琼脂培养基,待其凝固后倒置于霉菌培养箱中20-25℃培养72 h。每个菌种平行制备2个平皿,测定试验组菌落数。
同法测定供试品对照组、菌液对照组和阴性对照组菌落数。
按回收率=[(试验组平均菌落数-供试品对照组平均菌落数)/菌液对照组平均菌落数]计算回收率,结果(表4)。根据2015年版《中国药典》,采用平皿法时,回收率应在0.5-2范围内。可得出,黑曲霉需稀释至1∶10000,白色念珠菌需稀释至1∶1000000方能达到回收率要求。
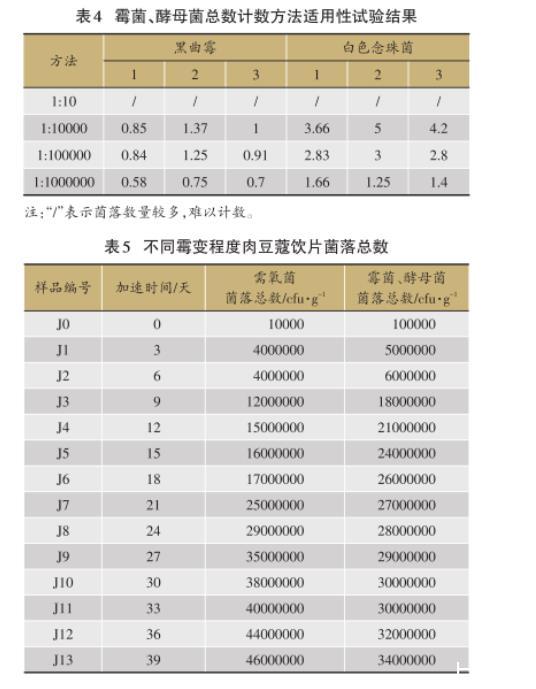
表4霉菌、酵母菌总数计数方法适用性试验结果
表5不同霉变程度肉豆蔻饮片菌落总数
2.5不同霉变程度样品菌落总数测定
综上,选用1∶1000、1∶10000、1∶100000、1∶1000000四个稀释度的供试液来测定不同霉变程度肉豆蔻饮片中需氧菌、霉菌及酵母菌的菌落总数。结果(表5)。显示,随着加速时间的延长,肉豆蔻样品中需氧菌菌落总数、霉菌、酵母菌菌落总数均呈上升趋势,且增长迅速。
3讨论
实验结果表明金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌及黑曲霉采用1:10普通平皿法进行方法适用性验证时,菌落数量较多,难以计数,不适合作为肉豆蔻饮片的微生物计数方法。经试验选用1∶1000、1∶10000、1∶100000、1∶1000000四个稀释度来进行肉豆蔻饮片微生物计数的方法学验证。其中金黄色葡萄球菌和枯草芽孢杆菌需稀释至1∶10000回收率可达到要求,而铜绿假单胞菌需稀释至1∶100000稀释级,才能达到回收率要求。黑曲霉和白色念珠菌分别在1∶10000、1∶100000稀释级时才能达到回收率要求。
通过对不同霉变程度肉豆蔻饮片微生物计数结果研究发现,随着加速时间的延长,肉豆蔻饮片霉变现象逐渐严重,且需氧菌和霉菌、酵母菌菌落总数均呈上升趋势,且加速0-6天时增长缓慢,6-9天呈爆发式增长,9-39天匀速增长。提示我们肉豆蔻作为常用药食两用药材在储藏过程中应实时监控其菌落总数,必要时增设微生物限度检查以保证用药的安全性与有效性。
有文献报道,中药饮片普遍受到多种微生物的污染,污染程度十分严重且污染的优势菌属大都是已知的产毒霉菌,因此在后续研究中应进一步研究肉豆蔻在霉变过程中产毒霉菌及控制菌的变化规律,及霉变产生的菌株对肉豆蔻饮片药效成分含量的影响,为建立更完善的肉豆蔻饮片质量标准提供依据。
相关新闻推荐
2、阿美替尼对结肠癌SW620、HT29细胞增殖、侵袭迁移和凋亡的作用及机制
3、豨莶草果实内生细菌分离、鉴定、生长特性、抑菌效果及药敏分析(二)
