胶滴肿瘤药敏检测技术检测及评价不同药物浓度的5'-DFUR对胃癌的疗效(二)
2结果
2.1 Primage图像分析结果
采用Primage图像分析系统对胶滴图像数据进行读取,原代肿瘤细胞团在胶滴内呈三维立体式增殖生长,与肿瘤细胞在人体内的生长环境相似。与加药组相比,Control组肿瘤细胞活性好,增殖较快;加药组呈现出不同程度的细胞凋亡,主要表现为细胞团变小且数量减少。(图2)
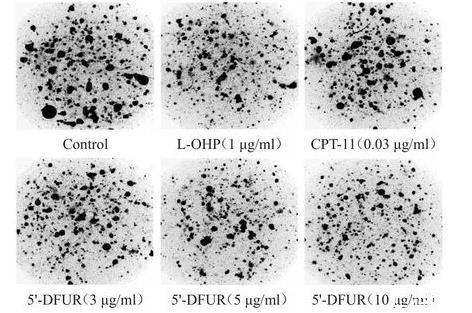
图2编号20170523-709标本的Primage图像分析结果(×40)
2.2实验组抗肿瘤药物的CD-DST检测结果
31例新鲜胃癌组织标本中,26例可评价,检测成功率为84%(26/31),5例检测失败原因为肿瘤细胞含量低,生长率低于0.8。检测成功的26例中,随着5'-DFUR浓度(3、5、10μg/ml)的增加,体外有效率(in vitro sensitivity,IVS)也呈增长趋势,高敏感IVS分别为23%、31%和46%(表2),由于已报道CAP单药的胃癌临床有效率约为30%,因此,本研究结果表明,胃癌体外药敏实验中,5μg/ml的5'-DFUR为CAP体外药敏检测CD-DST法的最适实验条件。

表2实验组抗肿瘤药物的CD-DST检测结果(n=26)
2.3验证组5'-DFUR的CD-DST检测结果
由于实验过程中的胃癌标本有限,为了进一步验证胃癌中5'-DFUR的IVS与CAP临床有效率的一致性,采用5μg/ml的5'-DFUR对另外34例胃癌标本进行了CD-DST法评价,其中1例检测失败,是由于肿瘤细胞量较少不足以检测;33例可评价,检测成功率为97%(33/34)。其中,高敏感IVS为30%(10/33),与实验组结果一致,即5μg/ml的5'-DFUR的IVS与CAP临床有效率一致。
3讨论
尽管临床诊断和治疗技术在不断提高,但胃癌由于其高度异质性、术后易复发和转移的特点,仍然是全球第三大癌症死亡原因。术后辅助化疗是胃癌治疗中的重要组成部分,目前一般采用经验性用药,但是由于肿瘤的异质性和患者的个体差异,导致疗效差异显著。随着肿瘤个体化治疗思想的提出,研究者建立了ATP生物荧光肿瘤体外药敏检测技术(ATP-tumor chemosensitivity assay,ATP-TCA)、MTT等体外药敏检测技术,但都存在一定的局限性。相较于上述方法,Kobayashi提出的CD-DST法具有原代细胞培养成功率高、需要的肿瘤细胞量少、临床相关性高、操作简单、培养时间短以及避免成纤维细胞干扰等优点。研究表明,CD-DST法对胃癌原代细胞在化疗药物敏感性检测中取得了较理想的结果。
CAP、5'-DFUR以及5-FU是临床上胃癌、结直肠癌辅助化疗的常用药,CAP与5'-DFUR以及5-FU相比,具有更好的安全性和有效性。但作为口服抗癌前体分子的CAP在肿瘤组织细胞内选择性地被TP代谢为5-FU,其疗效已经在多个临床试验中确定,而且毒性小于5-FU,口服比持续静脉注射更易被患者接受,因此,CAP可能是替代静脉注射5-FU的理想选择。在进展期胃癌的化疗中,CAP具有较高的抗癌活性,由于CAP的体外代谢受限,而5'-DFUR作为CAP重要的代谢产物,只需在肿瘤组织细胞中TP的作用下一步代谢即可转化为发挥抗肿瘤作用的5-FU。为了胃癌患者术后采用CD-DST法进行CAP体外药敏实验,本研究选择CAP的代谢产物5'-DFUR进行CAP的CD-DST药敏检测实验条件探索。研究结果显示,CD-DST法评价胃癌原代细胞对CAP的药敏条件检测结果稳定,胃癌原代细胞对不同浓度5'-DFUR的敏感度差异明显,5μg/ml的5'-DFUR在体外药敏实验条件检测中对胃癌的高敏感率为30%左右,这与文献报道的临床CAP单药一线治疗晚期胃癌的有效率一致。同时本研究结果显示抗肿瘤药物L-OHP和CPT-11的单药敏感率检测结果与实际临床单药治疗有效率相符。综上结果表明,采用CDDST法评价分析CAP在胃癌术后辅助化疗中的药敏检测条件对胃癌患者术后进行体外药敏实验及临床化疗药物的选择指导具有重要意义。
另有研究表明,CAP与第三代铂类抗肿瘤药物L-OHP联合用药对晚期胃癌疗效显著,且不良反应小,而CD-DST技术作为临床指导用药的重要参考,本实验室利用CD-DST法对CAP与L-OHP联合用药对肠癌原代细胞进行了体外药敏检测实验条件探索,初步结果显示,在肠癌中有效率约为55%,与文献报道的年龄较小患者临床有效率为58%和年龄较大患者临床有效率为52%一致性较高。而CAP与L-OHP联合用药对胃癌的IVS及其药敏检测实验条件正在进一步研究中。针对联合用药方案的CD-DST药敏检测实验条件及药敏实验是今后研究的方向,旨在为肿瘤患者术后进行体外药敏实验及临床化疗药物的选择指导提供重要参考。
