驴源马链球菌马亚种LXY019株的分离鉴定、生长曲线、致病性及耐药性分析(二)
1.7 分离菌的小鼠致病性试验
昆明小鼠25只,小鼠随机分成5组(I~V)。将活化好的驴源分离菌接种于4mL THB液体培养基中,37℃培养18h,用生理盐水将菌液稀释成4个浓度组(I组:1×10⁹CFU/mL; II组:1×10⁸CFU/mL; III组:1×10⁷CFU/mL; IV组:1×10⁶CFU/mL)及1个空白对照组(V组:生理盐水),各组按照每只0.5mL剂量进行腹腔注射。观察动物7d内的死亡状况,记录小鼠的临床症状(精神状态、被毛、饮食欲)及死亡情况,用改良Karber法计算分离菌对小鼠的半数致死量(LD50),绘制小鼠死亡曲线,称量小鼠体质量。
1.8 分离菌的毒力基因检测
表1 毒力基因引物序列
| 基因 Gene | 引物序列(5'→3') Primer sequence | 退火温度/℃ Annealing temperature | 片段大小/bp Size |
|---|---|---|---|
| lytA |
F TGAAGCGGGATTATCACTGGC R GCTAAACTCCCTGTATCAAGCG |
50 | 273 |
| hylB |
F CACCAATCCCCACTCTACTA R TGTGTCAAACCATCTATCAG |
55 | 503 |
| ply |
F CCCACTCTTCTTGCGGTTGA R TGAGCCGTTATTTTTCATACTG |
55 | 209 |
| seM |
F CAGAAAACTAAGTGCCGGTG R ATTCGGTAAGAGCTTGACGC |
54 | 521 |
| fneB |
F TTTAGGAGCGTCATCATCGTTAGG R TCAGGTGGCAAGGAAGAGGTC |
49 | 435 |
对驴源分离菌进行相关毒力基因鉴定,毒力基因及引物序列通过相关文献获取(表1),主要为链球菌自溶素(autolysin of Streptococcus pneumomiae, lytA)、透明质酸裂解酶(hyaluronidase, hylB)、链球菌溶血素(pneumolysin, ply)、类M蛋白(M-like protein, seM)和纤黏蛋白结合蛋白(Fibronectin Binding Protein, fneB),通过PCR进行鉴定。
1.9 分离菌的药物敏感性检测
将活化好的驴源分离菌、马源马链球菌马亚种(SEE-M)及标准菌ATCC9528菌液用生理盐水稀释至1×10⁶ CFU/mL。吸取100μL稀释好的菌液均匀涂布于THB固体培养基表面,采用K-B纸片琼脂扩散法,分析3株菌对氨苄西林、头孢噻肟、克拉霉素、红霉素、庆大霉素、阿米卡星、四环素、环丙沙星等药物的敏感性。设置3组平行对照,37℃孵育18~24h,用游标卡尺测量抑菌圈直径。
2 结果与分析
2.1 疑似菌的分离及镜检结果
从48份驴鼻拭子样品中共分离出1株疑似马链球菌,分离菌在50mL/L绵羊鲜血培养基上形成针尖大小、白色半透明、有明显β溶血特征的菌落(图1-A),革兰氏染色结果为阳性,显微镜下观察呈短链状(图1-B)。根据以上形态特征,笔者怀疑分离菌为马链球菌。
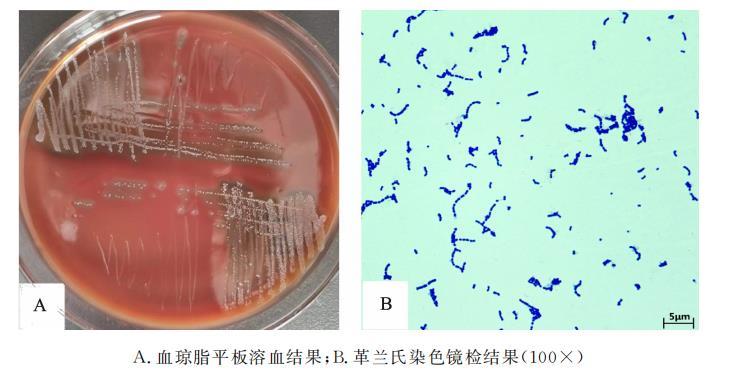
图1 分离菌菌落形态及镜检结果
2.2 分离菌16S rDNA序列扩增及测序分析
以分离菌株基因组DNA为模板,用细菌16S rDNA通用引物进行PCR扩增,在1466bp处出现特异性条带(图2),测序结果通过NCBI的BLAST比对发现,分离菌与已注册马链球菌马亚种的同源性达99.01%,结合菌落形态和染色镜检结果,确定该分离菌为马链球菌马亚种。
2.3 分离菌遗传进化树的绘制及分析
用MAGE7.0绘制遗传进化树,发现分离菌与新疆马链球菌马亚种HTP133(MT815602.1)遗传距离最近(图3),处于同一分支,将本次分离株命名为驴源马链球菌马亚种LXY019株。
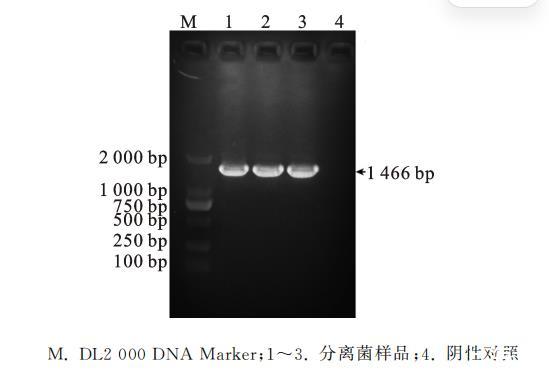
图2 分离菌 16S rDNA PCR扩增结果
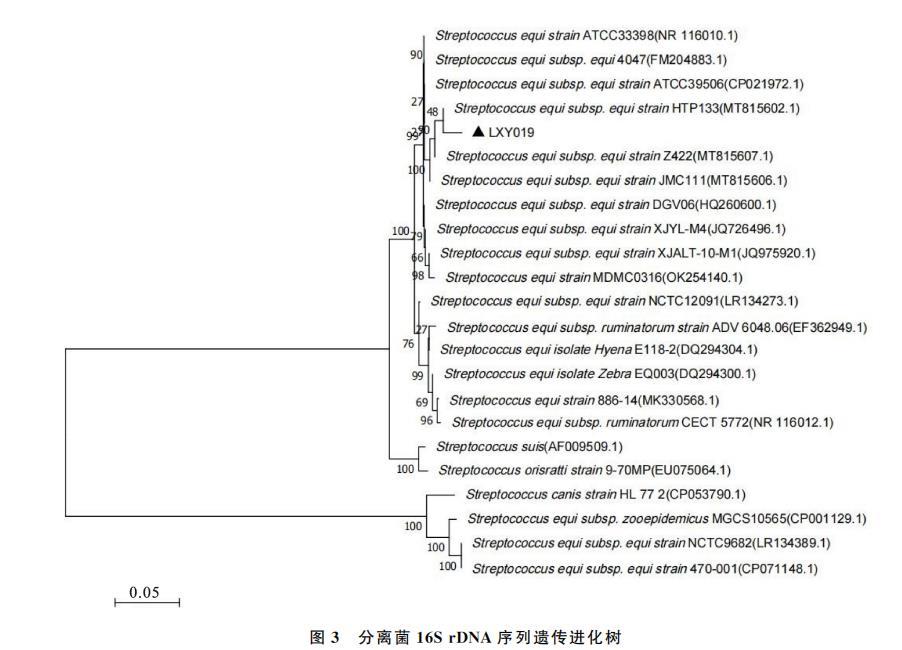
图3 分离菌 16S rDNA 序列遗传进化树
2.4 分离菌LXY019株的生长曲线
由生长曲线可知(图4),LXY019株接种8h为对数生长期,8h之后稳定生长,18h后进入衰亡期,SEE-M株于前8h呈对数生长,8h后稳定生长,呈衰亡趋势,但不明显,标准菌ATCC9528在THB液体培养基内前2h生长迅速,2h后缓慢生长,20h后呈衰亡趋势。
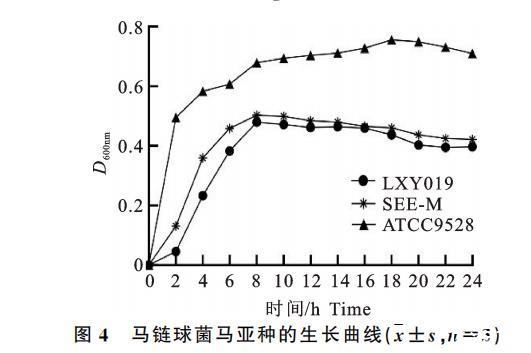
图4 马链球菌马亚种的生长曲线(x±s, n=3)
2.5 分离菌LXY019株对小鼠的致病性试验
表2 LXY019株对小鼠的致死率
| 组别 Group |
初始小鼠数 Number of initial mice |
死亡小鼠数 Number of death mice |
存活小鼠数 Number of live mice |
死亡率/% Mortality |
|||
|---|---|---|---|---|---|---|---|
| 1d | 2d | 3d~5d | 6d~7d | ||||
| I | 5 | 5 | — | — | — | 0 | 100 |
| II | 5 | 2 | 1 | 2 | 0 | 100 | |
| III | 5 | 0 | 0 | 0 | 0 | 5 | 0 |
| IV | 5 | 0 | 0 | 0 | 0 | 5 | 0 |
| V | 5 | 0 | 0 | 0 | 0 | 5 | 0 |
如表2所示,腹腔注射第1天,I组小鼠全部死亡;第2天,II组小鼠死亡2只,至第7天全部死亡;其余接种组(III组、IV组)小鼠均出现不同程度患病症状,如精神状态差,被毛粗乱,食欲废绝等,但至第7天未见死亡;V组小鼠无任何异常表现。剖检死亡小鼠,发现其肺泡充血严重,肝脏、肾脏和脾脏有不同大小的病灶,无菌采集死亡小鼠内脏涂擦于TSA平板上,37℃过夜培养,于心、肝、脾、肺、肾中分离到与LXY019株菌落形态大小一致的细菌菌落(图5)。
根据公式LD50=lg-1[Xm-i(ΣP-0.5)],计算得到分离菌LXY019株对小鼠的半数致死量为1.58×10⁷ CFU/mL。
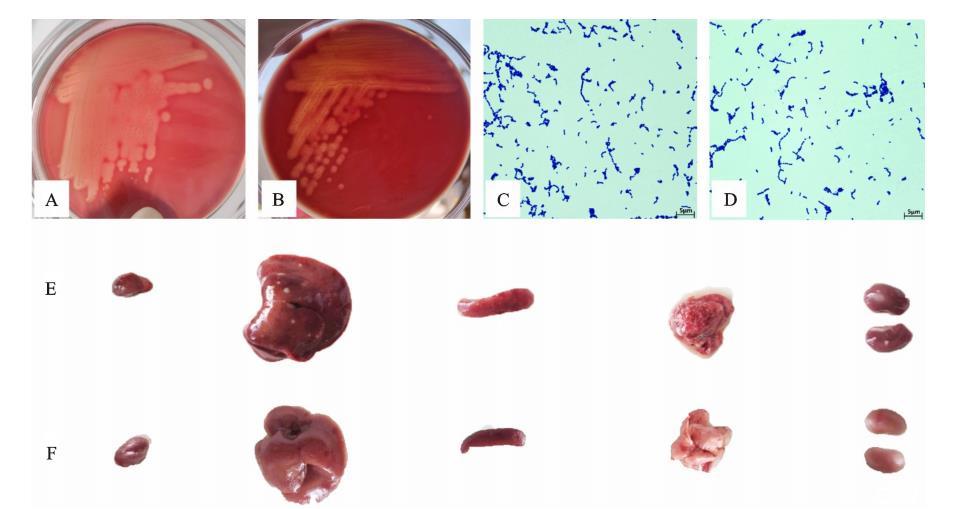
A、C.攻毒死亡小鼠内脏分离菌菌落形态及革兰氏染色结果(×100);B、D. LXY019株菌落形态及革兰氏染色结果(×100);E、F.攻毒死亡小鼠及健康小鼠内脏形态(依次为心、肝、脾、肺、肾)
相关新闻推荐
1、基于可培养技术的古象牙病害微生物分离鉴定与抑菌剂筛选评价(三)
