生活饮用水中微生物检测方法、菌落总数和肠球菌菌数定量分析(四)
2.4 定值结果分析
2.4.1 标准值计算
各定值实验室反馈的检测结果汇总见表5。定值实验室反馈的定值数据进行Grubbs检验并结合技术判断,所有数据无需剔除。经正态性检验结果可知,偏态系数A值均小于临界值,且峰态系数B均在所对应的临界值范围内,数据符合正态分布。经科克伦(Cochran)检验分析结果可知,科克伦准则的C值均小于C临界值,说明各组数据等精度。
| 检测项目 | 实验室编号 | 检测结果 (lg CFU)a | 平均值 | |||||
|---|---|---|---|---|---|---|---|---|
| 结果1-1 | 结果1-2 | 结果2-1 | 结果2-2 | 结果3-1 | 结果3-2 | |||
|
菌落总数 (lg CFU/mL) |
1 | 3.462 | 3.447 | 3.362 | 3.398 | 3.568 | 3.556 | 3.370 |
| 2 | 3.322 | 3.255 | 3.255 | 3.301 | 3.398 | 3.342 | ||
| 3 | 3.301 | 3.279 | 3.462 | 3.380 | 3.230 | 3.301 | ||
| 4 | 3.255 | 3.255 | 3.176 | 3.255 | 3.176 | 3.230 | ||
| 5 | 3.462 | 3.462 | 3.462 | 3.462 | 3.362 | 3.362 | ||
| 6 | 3.431 | 3.342 | 3.505 | 3.477 | 3.477 | 3.519 | ||
|
肠球菌 (lg CFU/100 mL) |
1 | 3.763 | 3.785 | 3.690 | 3.724 | 3.623 | 3.663 | 3.770 |
| 2 | 3.716 | 3.771 | 3.591 | 3.663 | 3.771 | 3.663 | ||
| 3 | 3.914 | 3.940 | 3.826 | 3.881 | 3.944 | 3.934 | ||
| 4 | 3.857 | 3.875 | 3.875 | 3.919 | 3.813 | 3.908 | ||
| 5 | 3.623 | 3.663 | 3.623 | 3.544 | 3.643 | 3.623 | ||
| 6 | 3.778 | 3.799 | 3.903 | 3.875 | 3.740 | 3.792 | ||
| a 注:各实验室通过oCelloScope微生物生长曲线分析系统或已验证的等效方法获得定量结果。 | ||||||||
a 注:各实验室通过oCelloScope微生物生长曲线分析系统或已验证的等效方法获得定量结果。
2.4.2 不确定度评估
经分析,标准样品不确定度的来源主要包括:因测定引起的标准不确定度(uchar)、因瓶间(不)均匀性引起的标准不确定度(ubb)和因长期(不)稳定性引起的标准不确定度(ults)。样品间不确定度采用样品间标准差即sbb = ubb,长期稳定性不确定度采用长期稳定性的样品间标准差即sbb = ults。合成标准不确定度依据公式(1)计算。各不确定度分量及合成标准不确定度见表6。
表6 各不确定度分量汇总| 不确定度来源 | 菌落总数 (lg CFU/mL) | 肠球菌 (lg CFU/100 mL) |
|---|---|---|
| 因测定引起的标准不确定度 uchar | 0.031 | 0.036 |
| 因瓶间(不)均匀性引起的标准不确定度 ubb | 0.012 | 0.018 |
| 因长期(不)稳定性引起的标准不确定度 ults | 0.016 | 0.021 |
| 合成标准不确定度 uCRM | 0.037 | 0.046 |
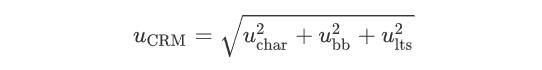
经统计计算及不确定度分析得到标准样品中菌落总数和肠球菌菌数的标准值及不确定度见表7。
| 定值信息 | 菌落总数 | 肠球菌 |
|---|---|---|
| 标准值 | 3.370 lg CFU/mL | 3.770 lg CFU/100 mL |
| 2300 CFU/mL | 5900 CFU/100 mL | |
| 合成不确定度 | 0.037 lg CFU/mL | 0.046 lg CFU/100 mL |
| 扩展不确定度 (k=2) | 0.074 lg CFU/mL | 0.092 lg CFU/100 mL |
| 特性值区间 (95%置信水平) | 3.296 ~ 3.444 lg CFU/mL | 3.678 ~ 3.862 lg CFU/100 mL |
| 2000 ~ 2800 CFU/mL | 4800 ~ 7300 CFU/100 mL |
3 讨论
本研究样品的制备采用了冷冻干燥技术制备。冷冻干燥是先将被干燥物料中的水冻成冰,然后使冰升华而除去水的一种干燥方法。由于其对细胞损伤小,特别适用于菌种干燥保存,而保护剂的使用能进一步降低损伤。本研究采用10%的海藻糖作为冻干保护剂,用0.5%的脱脂奶粉、1%聚乙二醇6000与冻干保护剂配制成基体溶液。将基体溶液与菌液充分混匀分装后,经过冷冻干燥的方式成功研制了生活饮用水中菌落总数和肠球菌的标准样品。
基于冷冻干燥技术的特点,样品可较好地保持样品基体的原有属性,使得其易于运输和储存,加水复溶后与新鲜样品状态一致。为确保标准样品的溯源性,本研究标准样品中添加的菌株均为标准菌株,经过验证符合要求。为了保证样品的均匀性,本研究选择的构成基体溶液的试剂均具有较好的水溶性,且在冻干前将菌液与基体溶液进行了充分混匀。按照GB/T 15000.3-2023《标准样品工作导则 第3部分:标准样品定值和均匀性与稳定性评估》的要求进行的均匀性分析的结果也表明,本研究制备的样品在95%置信概率下无显著差异,满足标准样品的要求。
所研制的样品为含有活的微生物的样品,极易发生变化(繁殖和死亡等),因此,样品基体中的水分、营养物质、包装形式及保存温度均是影响其稳定性的重要因素。本样品采用冷冻干燥法制备,水分含量较低,并采用西林瓶真空包装,因此基质及目标物在储存过程中不易发生显著变化。同时,鉴于微生物样品对温度敏感性较高的特性,温度越低,样品中目标物越稳定,因此本研究未开展低温运输条件下的稳定性研究。短期稳定性研究采用oCelloScope系统进行快速监测,结果表明,在模拟运输25、36 ℃条件下7 d,和42 ℃条件下5 d,标准样品中的菌落总数和肠球菌菌数结果无显著变化,样品具有良好的短期稳定性。长期稳定性研究结果表明,在-18 ℃条件下保存12个月后样品中菌落总数和肠球菌的量值均保持稳定,故为了保证样品特性量值的有效性,将样品有效期暂定为1年。采用多个实验室联合定值的方式对样品进行赋值,以此来保证标准样品量值的溯源性和准确性。综上,本研究制备的生活饮用水中菌落总数和肠球菌定量分析标准样品具有良好的稳定性,可实现在冷冻条件下长期稳定保存,适用于实验室日常检测中的质量控制,并有望拓展应用于快速检测方法评价、相关机构能力考核及快检方法研发等领域。
尽管本研究成功研制了生活饮用水中菌落总数和肠球菌定量标准样品,并通过优化保护剂和冷冻干燥工艺,标准样品在推荐储存条件下(-20 ℃)表现出良好的短期与较长时间的稳定性,但受微生物自身特性的影响,其长期稳定性仍需持续监测与数据更新。此外,运输稳定性研究基于模拟的理想运输条件开展,可能与实际物流过程中遭遇的温度波动或物理震荡存在差异,从而影响稳定性研究结果。另外,本研究制备的标准样品主要配套与现行有效的检测标准使用,并兼容oCelloScope等快速分析系统。随着分子生物学技术(如qPCR、数字PCR等)在微生物快速检测中的应用日益广泛,本标准样品是否同样适用于这些方法的校准与质量控制,均未在本研究范围内,这构成了未来研究的重要方向。
综上所述,本研究开发的标准样品为生活饮用水常规微生物检测的质量控制及量值溯源提供了重要的工具,但其有效应用需充分考虑其基质代表性、稳定性以及方法适用性等限制。未来的研究应致力于不断优化其制备工艺、稳定性及精准定值以及方法适用范围等方面,以推动饮用水微生物安全监测体系的进一步完善。
相关新闻推荐
1、多杀性巴氏杆菌分离鉴定、分型、药敏试验及小鼠致病性试验(四)
2、不同磁化水处理对有益微生物(苜蓿根瘤菌)生长及功能的影响——结果与分析
